Un equipo de científicos de la Universidad de Granada ha diseñado y patentado una nueva terapia, basada en nanopartículas (NPs) de poliestireno trifuncionalizadas y a partir de labioconjugación de diferentes moléculas, entre ellas la doxorrubicina, para tratar el cáncer de mama triple negativo y evitar los efectos adversos asociados a este fármaco. La investigación ha demostrado que se necesitan tres veces menos cantidad del fármaco usado en clínica con el nanosistema diseñado para producir el mismo efecto terapéutico que la quimioterapia actual, lo que claramente hace que sus efectos secundarios sean menores.
Un equipo de científicos de la Universidad de Granada (UGR) ha diseñado y patentado una nueva terapia, basada en nanopartículas (NPs) de poliestireno trifuncionalizadas y a partir de labioconjugación de diferentes moléculas, entre ellas la doxorrubicina, para tratar el cáncer de mama triple negativo y evitar los efectos adversos asociados a este fármaco. Este sistema ha sido patentado y publicado en la prestigiosa revista científica “Nanomedicine: Nanotechnology, Biology and Medicine”.

De izquierda a derecha, los autores de este trabajo: Juan Antonio Marchal Corrales, Rosario Sánchez Martin, Saúl A. Navarro Marchal, Victoria Cano Luque y Juan José Díaz Mochón.
El estudio ha sido realizado por un equipo de científicos liderado por la Rosario Sánchez Martin, del grupo de investigación NanoChemBio del centro Pfizer-Universidad de Granada-Junta de Andalucía de Genómica e Investigación Oncológica (Genyo) y el grupo CTS987: Desarrollo de estrategias terapéuticas y de diagnóstico de la Universidad de Granada, y Juan Antonio Marchal, del grupo de investigación ‘Terapias avanzadas: Diferenciación, Regeneración y Cáncer’ de la Universidad de Granada, ambos pertenecientes al Instituto de Investigación Biosanitaria de Granada (ibs.GRANADA) y a las Unidades de Excelencia de “Química aplicada a la Biomedicina y Medio Ambiente” y “Modeling Nature: from nano to macro” de la UGR.
La investigación se centra en la validación de una eficiente estrategia química para la bioconjugación de varias moléculas bioactivas de forma controlada en la NPy así llevar a cabo la producción de NPs de poliestireno trifuncionalizadas. Estas NPsestán funcionalizadas con un fármaco usado en los tratamientos de quimioterapia actual (doxorrubicina), un marcador fluorescente (fluoróforo) que permite la monitorización de las NPs, y un péptido de referencia (CRGDK), que les permite unirse específicamente a la neuropilina-1 (Nrp-1), un receptor de membrana que esta sobreexpresado en las células de cáncer de mama triple negativo humanas (TNBC) y no en las células sanas.
Esto permite dirigir las NPs cargadas del fármaco quimioterapéutico exclusivamente a las células tumorales, sin afectar a las sanas y, por otro lado, al estar unido el fluoróforo, localizar el tumor y hacer un seguimiento tanto de la eficacia del tratamiento como de la producción de metástasis, lo que las convierte en NP teranósticas (útiles tanto para diagnóstico como para tratamiento).
Eficaz ‘in vitro’ e ‘in vivo’
La eficacia del efecto de dichas NPs ha sido evaluada tanto in vitro como in vivo, utilizando un modelo de trasplante de células TNBC en la mama de ratonas, simulando de forma fidedigna el tumor de mama humano.
Los ensayos in vitro muestran que las NPs mejoran el índice terapéutico en comparación con la doxorrubicina libre, esto es, se necesitan tres veces menos cantidad del fármaco diseñado en la UGR para producir el mismo efecto terapéutico, que la quimioterapia actual, lo que claramente hace que sus efectos secundarios sean menores.
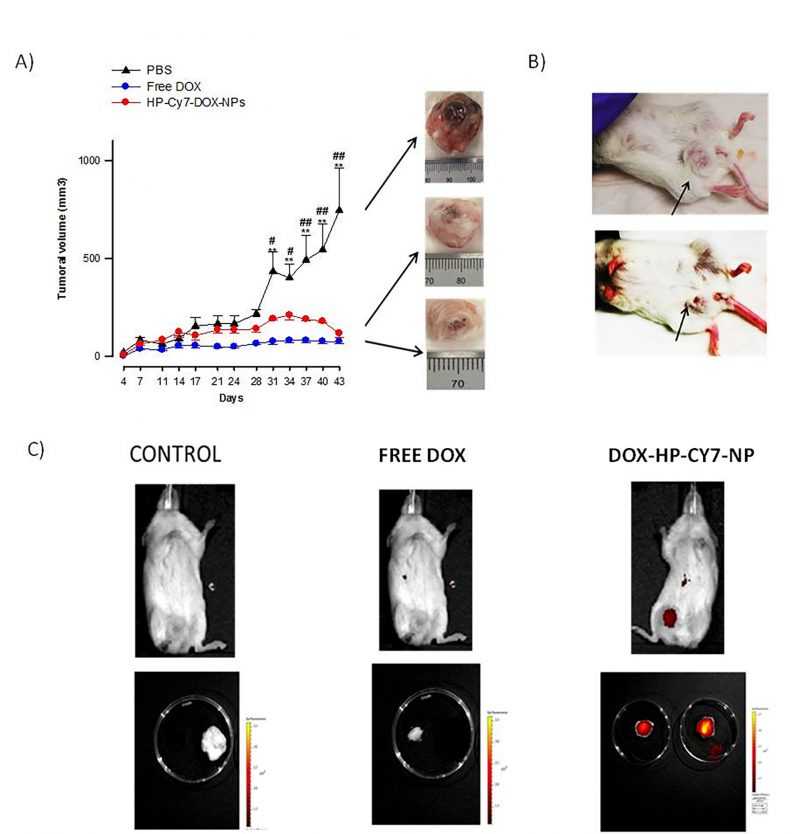
En la figura A, evolución del tamaño tumoral respecto al tiempo. En la figura B, el aspecto de los tumores en las ratonas. En la figura C, una imagen la capacidad teranósticade las NPs en las ratonas. La última imagen de la derecha muestra las ratonas tratadas con las NPstrifuncionalizadas y se observan estas NPs acumuladas específicamente en el tumor y de ahí su selectividad.
Los estudios in vivo muestran que las NP teranósticas van selectivamente dirigidas al área tumoral, reduciendo el volumen de este al mismo nivel que el tratamiento con doxorrubicina libre. Pero como ventaja en comparación a la doxorrubicina en solución, dichas NPs no presentan efectos secundarios, tales como la pérdida de peso, la toxicidad en el sistema nervioso o las lesiones cutáneas.
Este nano-dispositivo multifuncional basado en estrategias de bioconjugación ha demostrado ser un buen candidato para el diagnóstico y la monitorización de los tumores que sobre-expresan Nrp-1. Además, como ventaja adicional se encuentra que este nano-dispositivo versátil se puede adaptar fácilmente para tratar y controlar otros tipos de cáncer adaptando la estrategia de conjugación dependiendo del tipo tumoral.
El estudio ha sido financiado por el Ministerio de Ciencia, Innovación y Universidades (MICINN) y el Instituto de Salud Carlos III, además de la Oficina de Transferencia de la Investigación (OTRI) y la “Cátedra Dres. Galera y Requena de investigación en células madre cancerígenas” de la UGR.
Suscríbete a nuestra newsletter
y recibe el mejor contenido de i+Descubre directo a tu email





