Moderna, la segunda vacuna contra la COVID-19 autorizada en la Unión Europea
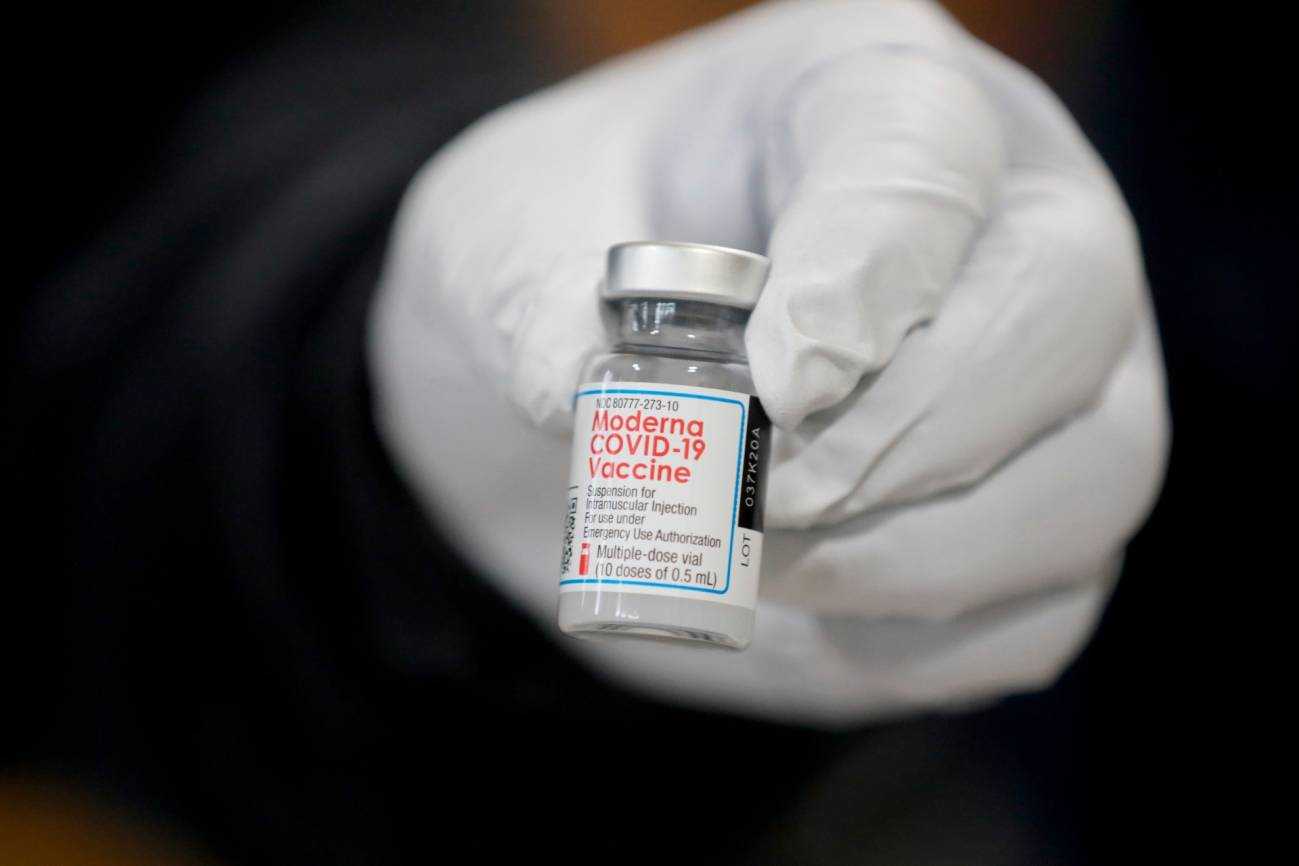
Tras el visto bueno de su Agencia de Medicamentos, la Unión Europea ha aprobado la comercialización de la vacuna de Moderna, que proporcionará 160 millones de dosis hasta el tercer trimestre de 2021. Es la segunda vacuna contra la COVID-19 que se distribuirá por la UE, después de la de Pfizer.
La Comisión Europea ha concedido este miércoles una ‘autorización condicional de comercialización’ para la vacuna contra la covid-19 desarrollada por Moderna, lo que la convierte en la segunda vacuna contra la covid-19 autorizada en la UE.
Esta autorización sigue una recomendación científica favorable basada en una evaluación minuciosa de la seguridad, la eficacia y la calidad de la vacuna por parte de la Agencia Europea de Medicamentos (EMA) y cuenta con el respaldo de los Estados miembros.
Moderna, con la que la Comisión firmó un contrato el 25 de noviembre, proporcionará un total de 160 millones de dosis entre el primer y el tercer trimestre de 2021. Esta cantidad se sumará a los 300 millones de dosis de la vacuna distribuida por Pfizer y BioNTech, la primera que fue autorizada en la UE, el 21 de diciembre de 2020.
“Estamos proporcionando a los europeos más vacunas contra la covid-19. Con la de Moderna tendremos otros 160 millones de dosis, pero habrá más vacunas. Europa ha asegurado el suministro de hasta 2 000 millones de dosis de posibles vacunas. Tendremos una cantidad más que suficiente de vacunas seguras y eficaces para proteger a todos los europeos”, ha declarado la presidenta de la Comisión Europea, Ursula von der Leyen.
El 30 de noviembre de 2020, Moderna presentó una solicitud de autorización de comercialización a la EMA, que ya había iniciado una revisión continua de los datos en noviembre. Gracias a esa revisión continua, la agencia ha ido evaluando la calidad, la seguridad y la eficacia de la vacuna a medida que se iba disponiendo de datos.
El Comité de Medicamentos de Uso Humano (CHMP) de la EMA ha evaluado minuciosamente los datos y ha recomendado por consenso que se conceda una autorización formal condicional de comercialización. Una autorización condicional de comercialización es uno de los mecanismos reglamentarios de la UE para facilitar el acceso temprano a medicamentos que cubren una necesidad médica no satisfecha, también en situaciones de emergencia como la actual pandemia.
Sobre la base del dictamen favorable de la EMA, la Comisión ha verificado todos los elementos que respaldan la autorización de comercialización y ha consultado a los Estados miembros antes de concederla.
“Todos estamos juntos y unidos en esto. Por eso hemos negociado la cartera de vacunas más amplia del mundo para todos nuestros Estados miembros. Hoy autorizamos una segunda vacuna segura y eficaz, de Moderna, la cual, junto con la de Pfizer-BioNTech, garantizará el despliegue de 460 millones de dosis a una velocidad cada vez mayor en la UE, y habrá más”, ha garantizado Stella Kyriakides, comisaria de Salud y Seguridad Alimentaria.
La vacuna de Moderna está basada en el ARN mensajero (ARNm), que desempeña un papel biológico fundamental, ya que transmite instrucciones del ADN a la maquinaria de producción de proteínas de las células. En una vacuna ARNm, estas instrucciones producen fragmentos inocuos del virus que el cuerpo humano utiliza para crear una respuesta inmunitaria a fin de prevenir o combatir la enfermedad.
Cuando se administra la vacuna a una persona, sus células leerán las instrucciones genéticas y producirán una proteína espicular, una proteína en la superficie exterior del virus que este utiliza para introducirse en las células del organismo, reproducirse y causar la enfermedad. A continuación, el sistema inmunitario de la persona tratará esta proteína como extraña y producirá defensas naturales (anticuerpos y linfocitos T) contra ella.
Suscríbete a nuestra newsletter
y recibe el mejor contenido de i+Descubre directo a tu email