España /
12 de enero de 2026
Crean el primer atlas celular de la inflamación que utiliza IA para acelerar el diagnóstico de enfermedades inflamatorias
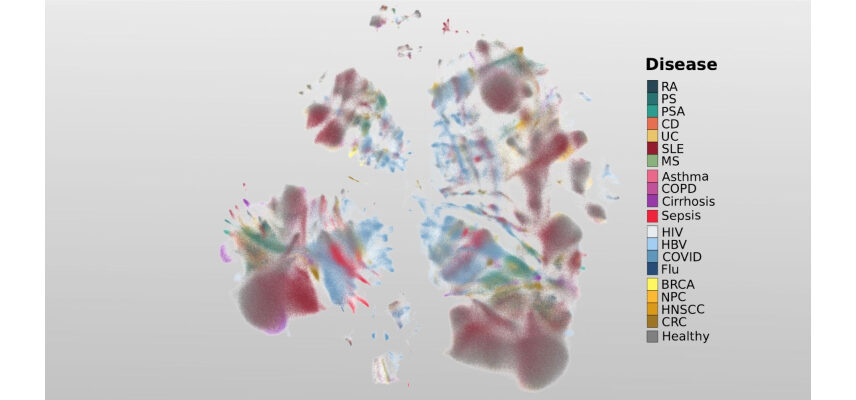
Investigadores del Centro Nacional de Análisis Genómico han lanzado esta herramienta biomédica, una base de datos exhaustiva en la que han analizado más de 6,5 millones de células de la sangre procedentes de 1.000 personas, tanto individuos sanos como pacientes de 19 enfermedades diferentes.
La inflamación es una parte natural de la vida cotidiana. Cuando te raspas la rodilla o te resfrías, tu cuerpo genera una respuesta inflamatoria para restablecer el equilibrio y reparar los tejidos, un proceso esencial para mantener la salud. Sin embargo, en muchas enfermedades, esta respuesta se ve interrumpida. Cómo falla la inflamación y cómo estos cambios difieren entre afecciones como infecciones como la COVID-19, enfermedades inmunológicas como la psoriasis o la artritis reumatoide y cánceres como el de mama o el colorrectal, sigue siendo poco conocido. Para arrojar luz sobre esta pieza faltante, investigadores del Centro Nacional de Análisis Genómico (CNAG), en colaboración con la École Polytechnique Fédérale de Lausanne (EPFL, Suiza) , han creado el primer atlas celular de la inflamación, un recurso integral basado en más de 6,5 millones de células sanguíneas de más de 1000 individuos sanos y pacientes que abarcan 19 enfermedades diferentes.
Publicado en la prestigiosa revista Nature Medicine, este estudio presenta un enfoque innovador: considerar las células mismas como un biomarcador que puede ayudar a desvelar algunos de los misterios que se esconden tras las enfermedades inflamatorias. «Las células inmunitarias de la sangre contienen huellas dactilares de enfermedades, que detectan al circular por nuestro sistema. Su lectura con resolución celular nos permite convertir las células en biomarcadores vivos para diagnósticos de precisión», explica el Dr. Holger Heyn, autor principal y correspondiente del estudio y líder del Grupo de Genómica de Células Únicas del CNAG. «Ofrecemos la prueba de concepto para convertir las células inmunitarias en una herramienta de diagnóstico universal, un concepto que ahora estamos desarrollando en la fase de prototipo clínico».
La investigación examina las señales inflamatorias de las células inmunitarias en la sangre y lo que pueden revelar sobre las enfermedades que afectan a los pacientes. Al analizar en detalle los diferentes estados de las células inmunitarias que impulsan la progresión de la enfermedad, el estudio revela cómo cambia la inflamación en diferentes afecciones. Utilizando el nuevo atlas celular, los investigadores identificaron indicadores moleculares que actúan como indicadores, guiando el camino hacia una comprensión más profunda de la biología subyacente y la clasificación precisa de estas enfermedades. Para encontrar estos indicadores, los investigadores profundizaron en los genes inflamatorios que orquestan la respuesta inmunitaria, identificando programas que activan las células inmunitarias, guían su movimiento, defienden contra agentes dañinos y desencadenan la defensa. Este conocimiento genético ayuda a distinguir cada enfermedad y a clasificar a los pacientes según sus características inflamatorias únicas.
Por ejemplo, en el lupus eritematoso sistémico, una enfermedad autoinmune agresiva, los mapas revelaron que ciertos estados de las células inmunitarias están vinculados a formas más graves de la enfermedad. Una de las señales clave implicadas es la respuesta al interferón, un mecanismo de defensa natural que suele ayudar a combatir los virus. En el lupus, esta señal está constantemente activa, lo que puede sobreestimular el sistema inmunitario y agravar la inflamación. Este descubrimiento ayuda a los investigadores a comprender por qué algunos casos se vuelven crónicos y más agresivos.
De los mapas al significado: cómo la IA aprende de la inflamación
Además de utilizar las últimas técnicas de genómica unicelular del CNAG, el estudio introduce una segunda innovación importante: la aplicación de IA para clasificar a los pacientes basándose en datos unicelulares. Los investigadores desarrollaron un modelo de IA generativa capaz de aprender de los estados celulares y la actividad genética capturados en el atlas, con el objetivo de proyectar los patrones biológicos a futuros pacientes. Este nuevo enfoque sienta las bases para una herramienta de medicina de precisión que podría acelerar el diagnóstico y guiar tratamientos más personalizados, mejorando así la calidad de vida y el manejo clínico de las personas afectadas por enfermedades inflamatorias.
El Dr. Juan Nieto, inmunólogo del Grupo de Genómica de Células Únicas del CNAG y coautor del estudio, destaca: «Este atlas nos ayuda a avanzar hacia una atención más personalizada. Al comprender los patrones inflamatorios específicos de cada paciente, los médicos podrán elegir tratamientos de forma más temprana y precisa, reduciendo el ensayo y error y mejorando la atención al paciente».
Tras el lanzamiento de este recurso de código abierto, que ya se ha probado con muestras de pacientes como herramienta de diagnóstico personalizado, los investigadores trabajan ahora en la siguiente fase del proyecto. Sus esfuerzos se centran en establecer los protocolos necesarios para garantizar la calidad y la estandarización, con el objetivo de sentar unas bases sólidas que permitan su integración en la práctica clínica y, en el futuro, su acceso a hospitales e instituciones sanitarias.
El estudio ha sido posible gracias a los datos de DocTIS , un proyecto multicéntrico financiado por la Unión Europea cuyo objetivo es mejorar la eficacia del tratamiento en enfermedades inflamatorias inmunomediadas, y a la colaboración de una red de hospitales nacionales y europeos.
Referencias:
Jiménez-Gracia, Laura, et al. ‘Paisaje interpretable de la inflamación en células inmunitarias circulantes’. Nature Medicine, enero de 2026, pp. 1–12. www.nature.com , https://doi.org/10.1038/s41591-025-04126-3 .
Suscríbete a nuestra newsletter
y recibe el mejor contenido de i+Descubre directo a tu email






