PKAN es uno de los quince subtipos del grupo de enfermedades raras denominadas NACH, producidas por la acumulación de hierro
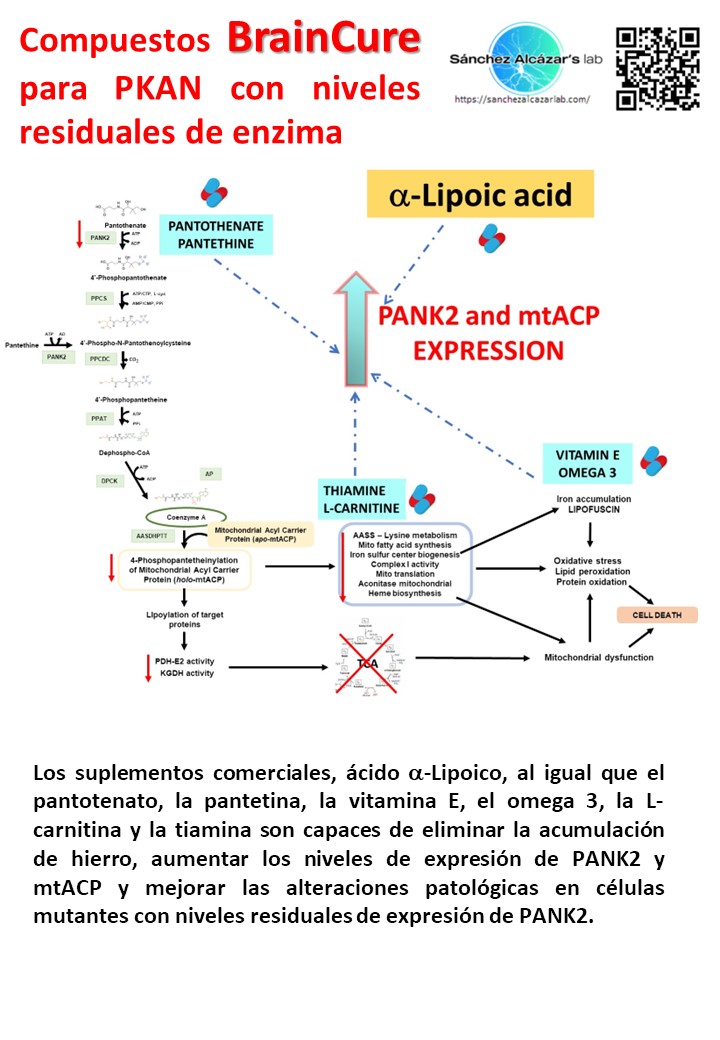
El equipo científico de la Universidad Pablo de Olavide dirigido por el catedrático José Antonio Sánchez Alcázar ha publicado recientemente un estudio en la revista internacional Orphanet Journal of Rare Diseases en el que demuestra que el ácido alfa lipoico corrige significativamente el fenotipo mutante en modelos celulares de PKAN. La suplementación con ácido alfa lipoico fue capaz de eliminar la acumulación de hierro y mejorar las alteraciones patológicas en las células mutantes con niveles de expresión residuales del enzima mutado.
PKAN es uno de los quince subtipos de la enfermedad rara denominada neurodegeneración con acumulación de hierro (NACH o NBIA por sus siglas en inglés) que afecta principalmente a niños y niñas en su primera década de vida. Las NACHs son un grupo de trastornos neurológicos hereditarios en los que el hierro se acumula en los ganglios basales, lo que produce distonía progresiva, espasticidad, parkinsonismo, anomalías neuropsiquiátricas, atrofia óptica o degeneración de la retina, y a menudo la muerte temprana de los afectados. La forma más prevalente de NACH es la neurodegeneración asociada a pantotenato quinasa (PKAN), asociada con mutaciones en el gen de la pantotenato quinasa 2 (PANK2) que es esencial para la síntesis de coenzima A (CoA). No existe cura para la PKAN, ni existe un tratamiento estándar.

Equipo científico de la Universidad Pablo de Olavide dirigido por el catedrático José Antonio Sánchez Alcázar
Con el apoyo del Instituto de Salud Carlos III, la Junta de Andalucía, la Fundación MERCK Salud y la Federación Española de Enfermedades Raras, el equipo de investigación de la UPO ha identificado que el ácido alfa lipoico es capaz de eliminar la acumulación de hierro y aumentar los niveles de expresión del enzima mutante PANK2. De esta manera, el aumento de los niveles de expresión del enzima mutante se asoció con una mejora significativa en las principales alteraciones patológicas de las células PKAN. La suplementación con ácido alfa lipoico puede ser de ayuda para el tratamiento de pacientes con PKAN con niveles de expresión residual de PANK2.
El ácido alfa lipoico se produce de forma natural en el cuerpo y es necesario para el crecimiento celular, la actividad mitocondrial y la coordinación del metabolismo energético, así como para regular la transcripción de muchos genes. Se caracteriza por su poder antioxidante; es por ello que posee propiedades neuroprotectoras y antiinflamatorias. En este sentido, el ácido alfa lipoico puede reducir los factores proinflamatorios y eliminar las especies reactivas de oxígeno y nitrógeno, así como restaurar la función mitocondrial y reducir el daño celular. Además, se ha demostrado que el ácido alfa lipoico reduce la peroxidación lipídica y aumenta la actividad antioxidante celular. Varios estudios han demostrado que este ácido también tiene un efecto quelante sobre metales como el hierro, reduciendo la acumulación de hierro en la corteza cerebral y un impacto positivo sobre el estrés oxidativo.
En cuanto a su uso médico, el ácido alfa lipoico es uno de los antioxidantes más eficientes debido a su buena biodisponibilidad, capacidad de atravesar la barrera hematoencefálica y la falta de efectos tóxicos a dosis terapéuticas. Muchos estudios clínicos han demostrado el efecto beneficioso de ácido alfa lipoico en muchas afecciones patológicas como diabetes, aterosclerosis, enfermedades cardíacas, cataratas y enfermedades neurodegenerativas. Por todas las razones mencionadas anteriormente, el ácido alfa lipoico es un candidato prometedor para el tratamiento de enfermedades neurodegenerativas como PKAN.
Proyecto BRAINCURE
Esta investigación se enmarca en el Proyecto BrainCure, desarrollado por el equipo científico dirigido por José Antonio Sánchez Alcázar, del Departamento de Fisiología, Anatomía y Biología Celular de la UPO. Desde que se pusiera en marcha en 2014, el equipo del profesor Sánchez Alcázar, que desarrolla su trabajo en el Centro Andaluz de Biología del Desarrollo (CABD), ha logrado grandes avances. Estos científicos y científicas proponen una visión ambiciosa y adaptada al nuevo concepto de medicina personalizada. Así, su trabajo se centra en evaluar la efectividad terapéutica de los distintos tratamientos en los fibroblastos derivados de los pacientes y en las células neuronales generadas por reprogramación directa.
Las evaluaciones personalizadas en modelos celulares derivados de pacientes pueden ser útiles para evaluar el comportamiento de mutaciones particulares bajo diferentes opciones terapéuticas y, por lo tanto, seleccionar los suplementos y las concentraciones de dosis más efectivos teniendo en cuenta sus propiedades farmacocinéticas. De esta manera, los resultados obtenidos en el laboratorio con modelos celulares de los propios pacientes podrán ser trasladado a la clínica para la realización de ensayos clínicos controlados.
En la actualidad el Proyecto BrainCure está realizando medicina de precisión en los 5 subtipos más frecuentes: PKAN, neurodegeneración asociada a pantotenato kinasa, con mutaciones en el gen PANK2; PLAN, neurodegeneración asociada a PLA2G6, con mutaciones en el gen PLA2G6; BPAN, neurodegeneración asociada a la proteína beta-propeller, con mutaciones en el gen WDR45; MPAN, neurodegeneración asociada a la proteína de la membrana mitocondrial, con mutaciones en el gen C19orf12; y FAHN, neurodegeneración asociada a la hidroxilasa de ácidos grasos, con mutaciones en el gen FA2H.
Este equipo científico está realizando actualmente medicina personalizada en más de 40 pacientes procedentes de España y otros países como Brasil, Colombia, México, EEUU, Francia, Reino Unido, Holanda, Hungría y Polonia.
Suscríbete a nuestra newsletter
y recibe el mejor contenido de i+Descubre directo a tu email